Каждую субботу новый выпуск из трех опытов!!!
Добро пожаловать на интерактивную страничку НЕО-кухня сайта школы!!!
Здесь мы с вами научимся делать увлекательные опыты и эксперименты
1.
- Очистка воды от механических примесей. Для опыта потребуется две стеклянных баночки (например, из-под майонеза). Очистке будем подвергать воду, загрязненную акварельными красками или гуашью. Наверняка мы хотя бы изредка пользуемся этими красками для рисования, а кисточки для рисования приходится часто мыть в воде. Бывает, что красками рисует младший брат или сестра...
 Чтобы сделать воду снова прозрачной, надо отфильтровать
механические примеси (частицы краски). Для этого потребуется воронка
(стеклянная или пластмассовая) и фильтровальная бумага. Если
фильтровальной бумаги нет, подойдет и газетная бумага.
Чтобы сделать воду снова прозрачной, надо отфильтровать
механические примеси (частицы краски). Для этого потребуется воронка
(стеклянная или пластмассовая) и фильтровальная бумага. Если
фильтровальной бумаги нет, подойдет и газетная бумага.
Свернем из фильтровальной бумаги (или из газеты) фильтр - так, как это
показано на рисунке. Этот фильтр поместим его в воронку, после чего
процедим (отфильтруем) загрязненную воду и получим воду прозрачную ...
Получилось?
А теперь проделайте все то же самое, но вместо фильтровальной (или
газетной) бумаги сделайте фильтр из туалетной бумаги или бумажной
салфетки. Удается ли с помощью такого фильтра избавиться от частиц
краски в воде? Если нет, то как вы думаете, почему?
А можно ли будет путем фильтрования удалить из соленой воды поваренную соль?
2.
- Опыт первый. Возьмем стакан или чашку, поместим туда
кусочек мела и добавим столового уксуса. Смесь тотчас "закипает" - в
результате химической реакции мела (карбоната кальция) с уксусной
кислотой (входящей в состав столового уксуса - водного раствора этой
самой уксусной кислоты) получился углекислый газ.

Интересно, а будет ли выделяться углекислый газ, если столовый уксус предварительно разбавить водой вдвое? впятеро? в десять раз? Если заменим столовый уксус раствором лимонной кислоты (1 чайная ложка на стакан воды) или соком, выжатым из свежего лимона? Что будет наблюдаться, если вместо мела мы возьмем питьевую соду (гидрокарбонат натрия), кусок природного известняка или осколок мрамора?
Вопросы. Специалисты по охране окружающей среды часто говорят об опасности "кислотных дождей". Что в большей степени подвержено разрушению под действием кислотного дождя - гранитная, бронзовая или мраморная статуя, находящаяся под открытым небом? Известно, что накипь внутри чайника состоит из карбоната кальция, а избавиться от нее можно с помощью столового уксуса. Как это сделать практически? Напишите "инструкцию для домохозяйки" по удалению накипи столовым уксусом.
- Опыт второй. Для этого опыта попросим у мамы ломтик картофеля и настойку иода
из аптечки. Капнем настойкой на картошку и увидим, что бурый цвет иода
превратился в темнофиолетовый. Здесь происходит химическая реакция между
иодом и крахмалом, который содержится в картофеле, и получается
новое вещество сине-фиолетового цвета. Химики используют эту реакцию для
того, чтобы установить, содержится ли в том или ином пищевом продукте
крахмал, а если содержится - то в каком количестве.

Приготовим для опыта картофель и яблоко 

Чтобы опыт был более наглядным, к иодной настойке можно добавить иодид калия.
Для опыта нужны свежие срезы овощей и фруктов!

Иодное пятно на срезе картофеля заметно ярче, чем на яблоке - значит, в картофеле крахмала больше 
Давайте проверим, какие из овощей, фруктов и других пищевых продуктов содержат это полезное вещество крахмал, а какие - нет. Для этого нанесем капельку иодной настойки на кусочек хлебного мякиша, ломтики моркови, яблока или груши, свежий срез арбуза или дыни, на муку (предварительно надо смешать ее с водой). Исследуем таким же способом манную и рисовую крупу, молоко, сахар, поваренную соль... Придумайте сами, что еще можно взять на кухне для нашего исследования - конечно, с разрешения родителей.
Вопрос. Перечислите пищевые продукты, которые, согласно нашему исследованию, а) содержат крахмал, б) не содержат крахмала.
- Опыт третий. Третий опыт тоже по силам любому, кто начинает изучать химию. Возьмем немного (одну чайную ложку) питьевой соды
- гидрокарбоната натрия - и зальем в стакане горячей водой. Тотчас
начнется бурное выделение углекислого газа: питьевая сода (гидрокарбонат
натрия) превращается в "стиральную" соду (карбонат натрия). Потом в
стакан добавим спиртовой раствор фенолфталеина (этот
кислотно-основный индикатор совсем недавно использовали как сильное
слабительное средство "пурген"). И бесцветная смесь в стакане тут же
окрасится в ярко-розовый цвет. Химическая реакция между содой, водой и
фенолфталеином приводит к образованию веществ, обладающих характерной
окраской. Такая окраска указывает на щелочную среду водного раствора
соды.
Посмотреть видеозапись опыта cкачать zip(~6.6Mб)



Теперь можно продолжить опыт: к розовому раствору соды, содержащему фенолфталеин, медленно, по капельке, добавлять столовый уксус. Раствор будет постепенно обесцвечиваться, так как щелочь и кислота (раствор соды и раствор уксуса) реагируют между собой и превращаются в соль (ацетат натрия) и воду. Вдобавок вы снова увидите бурное выделение углекислого газа...
Посмотреть видеозапись опыта cкачать zip(~7.3Mб)
Вопрос. С помощью веществ, участвующих в данном опыте, можно сделать на бумаге невидимую надпись, а потом "проявить" и прочитать ее. Как это осуществить практически? Напишите подробное описание такого опыта, а потом, пользуясь этим описанием, проделайте сам опыт. Получилось?..
3.
- Выращивание кристаллов медного купороса, хромокалиевых квасцов и поваренной соли.
Если не дожидаться у моря погоды и смены времен года, можно за две-три недели вырастить красивые кристаллы солей у себя дома. Для этого потребуется стеклянная банка, проволочка и нитка, да еще необходимый запас соли, кристаллы которой вы собираетесь выращивать. Очень эффектно выглядят "доморощенные" кристаллы медного купороса ярко-синего цвета и хромокалиевых квасцов (фиолетовые), хороши и бесцветные кубики поваренной соли.
Сначала приготовим как можно более концентрированный раствор выбранной соли, внося соль в стакан с водой, - до тех пор, пока очередная порция соли не перестанет растворяться при перемешивании. После этого слегка подогреем смесь, чтобы добиться полного растворения соли. Для этого стакан поставим в кастрюлю с теплой водой.
Полученный концентрированный раствор перельем в банку или химический стакан; туда же с помощью проволочной перемычки (можно также сделать перемычку из стержня шариковой ручки) подвесим на нитке кристаллическую "затравку" - маленький кристаллик той же соли - так, чтобы он был погружен в раствор. На этой "затравке" и предстоит расти будущему экспонату вашей коллекции кристаллов.
Химический стакан с насыщенным раствором поваренной соли и нитка с "затравкой" для роста кристаллов. Через трое суток после начала опыта (фото справа) нитка, опущенная в насыщенный раствор, превратилась в "ожерелье" из кристаллов хлорида натрия.



Химический стакан с раствором медного купороса и нитка с "затравкой" для выращивания кристаллов. Через трое суток после начала опыта на нитке появился кристалл медного купороса, похожий на другоценный камень.



Сосуд с раствором поставим в открытом виде в теплое место. Когда кристалл вырастет достаточно большим, вынем его из раствора, обсушим мягкой тряпочкой или бумажной салфеткой, обрежем нитку и покроем грани кристалла бесцветным лаком, чтобы предохранить от "выветривания" на воздухе.
Обратите внимание на цвет и форму полученных кристаллов.Так будет выглядеть кристалл медного купороса, выращенный из раствора.

Выпуск от 10.12.11
Опыты с содой и уксусом для детей


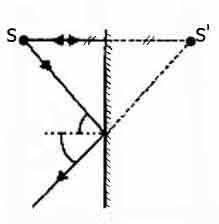
См. также: Опыты и эксперементы с водой для детей Выпуск от 17.12.11 ПЛОСКОЕ ЗЕРКАЛО Как же формируется изображение предмета в зеркале? Построим изображение
точечного источника света (S) в зеркале. Для этого достаточно проследить
Берем самый простой для построения луч - луч, падающий перпендикулярно
на поверхность зеркала, Изображение в плоском зеркале мнимое ("за зеркалом"), прямое (неперевернутое), в натуральную величину и расположено симметрично
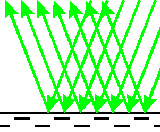
источнику относительно плоскости зеркала. Большинство зеркал изготавливается из очень гладкого стекла,
покрытого с обратной стороны
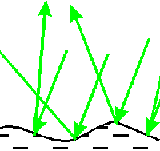
Если поверхность зеркала изогнутая , то изображение будет искаженным ("кривое зеркало"). Совсем другое отражение получается от шероховатой поверхности.
НЕ МОЖЕТ БЫТЬ !
При жизни Ньютон более всего был известен своими исследованиями
в области оптики. В Сиракузах, где по легенде Архимед поджигал с помощью зеркал вражеские корабли, ему был установлен памятник, изображающий ученого
со сферическим зеркалом в руках, направленным Леонардо да Винчи писал свои трактаты перевернутым шрифтом с помощью зеркала. ___ Первый оптический семафорный телеграф связал в конце 17 века
Париж с городом Лиллем. ___ Живые зеркала – светящиеся в темноте глаза кошки или блестящая
рыбья чешуя, переливающаяся ___ ОПЫТЫ 1. Опыты с зеркалом.
___ Получите пучок параллельных лучей с помощью фонарика и расчески,
расположив их
ЗАГЛЯНИ
Человек приближается к зеркалу со скоростью 1м/с. ___ Можно ли вместо белого экрана в кинотеатрах использовать плоское зеркало? ___ В плоском зеркале видно изображение свечи. Что с ним произойдет, если между зеркалом ВСЕ НА ПРИРОДУ! Интересно, можно ли с помощью "солнечных зайчиков" вскипятить воду?
|
опыт от 24.12.11гг
1. Обнаружение белков. В пробирку наливают 1 мл растаявшего молочного мороженого и добавляют 5–7 мл дистиллированной воды. Пробирку закрывают пробкой и встряхивают. К 1 мл полученной смеси добавляют 1 мл 5-10 % раствора NaOH и несколько капель 10 % раствора CuSO4. Содержимое пробирки встряхивают. Происходит биуретовая реакция. при этом появляется ярко-фиолетовое окрашивание, связанное с взаимодействием пептидных связей белковых молекул со свежеосажденным Cu(OH)2:

Обнаружение лимонной кислоты (пищевой добавки Е330) в плодово-ягодном мороженом. В пробирку налейте 1 мл растаявшего мороженого и добавьте 1 мл насыщенного раствора пищевой соды. Наблюдается появление пузырьков углекислого газа из-за протекания следующей реакции:
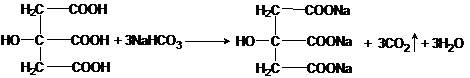
Обнаружение углеводов в молочном мороженом. Мороженое на молочной основе содержит дисахариды лактозу и сахарозу. В пробирку налейте 1 мл такого мороженого и добавьте 5–7 мл дистиллированной воды. Пробирку закройте пробкой и встряхните несколько раз. Профильтруйте полученную смесь и к фильтрату добавьте 1 мл 5-10 % раствора NaOH и 2–3 капли 10 % раствора CuSO4. Содержимое пробирки осторожно встряхните. Образуется ярко-синий раствор комплексного соединения сахарозы и лактозы с медью(II). Это качественная реакция на многоатомные спирты:
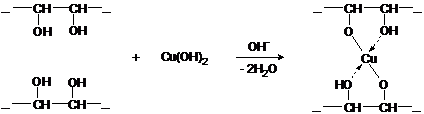
Полученный раствор нагрейте на спиртовке. Лактоза, находясь в нециклической (альдегидной) форме реагирует с Cu(OH)2. При этом образуются различные продукты окисления и деструкции лактозы. Cu(OH)2 восстанавливается до оранжевого CuOH, который потом разлагается до Cu2O красного цвета. В ходе реакции может выделиться и медь. Упрощенно процесс можно представить следующими уравнением:
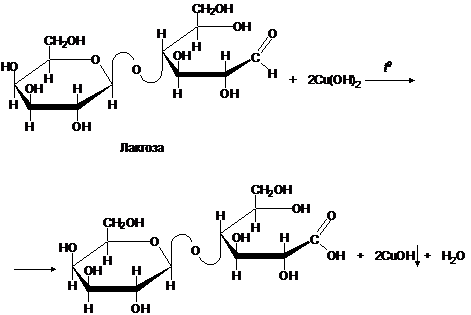
2CuOH ![]() Сu2O
+ H2O.
Сu2O
+ H2O.
Обнаружение сахарозы в плодово-ягодном мороженом. В плодово-ягодном мороженом содержится сахароза. В пробирку наливают 1 мл растаявшего мороженого и 1 мл 5-10% раствора NaOH. Затем приливают 2–3 капли 10 % раствора CuSO4. Наблюдают ярко-синее окрашивание (качественная реакция на многоатомные спирты).
2.
Обнаружение сахарозы. Возьмите небольшой кусочек шоколада и мелко настругайте его ножом. При обращении с ножом будьте осторожны! Шоколадную стружку насыпьте в пробирку на высоту примерно 1 см. Добавьте к шоколаду 2-3 мл дистиллированной воды. Содержимое пробирки несколько раз хорошо встряхните и профильтруйте. К фильтрату добавьте 1 мл 5–10% раствора NaOH и 2–3 капли 10 % раствора CuSO4. Пробирку встряхните. Происходит ярко-синее окрашивание. Реакцию дает сахароза, являющаяся многоатомным спиртом.
Сахарное поседение шоколада. Несколько кусочков шоколада слегка опрыскивают водой, заворачивают в фольгу и помещают на 1–2 недели в холодильник (не в морозильное отделение). Со временем на поверхности шоколада появится белый налет. Это выступили кристаллики сахарозы. Смывают налет 3–5 мл дистиллированной воды и обнаруживают в полученном растворе сахарозу. Для этого к раствору приливают 1 мл 5-10 % раствора NaOH и 1–2 капли 10 % раствора CuSO4. Смесь взбалтывают. Появляется характерное ярко-синее окрашивание (качественная реакция на многоатомные спирты).
3.
Свойства красителей, входящих в состав жвачки. Окрашенную жевательную резинку, порезанную на небольшие кусочки, помещают в пробирку и приливают 2–3 мл дистиллированной воды. Пробирку нагревают в пламени спиртовки до получения окрашенного раствора. Раствор разливают по двум пробиркам и добавляют в одну из них 1 мл 5-10 % раствора HCl или H2SO4, а в другую – 1 мл 5-10 % раствора NaOH. В зависимости от вида красителя будет происходить изменение его окраски в кислой и щелочной средах.
Обнаружение подсластителей. В пробирку помещают порезанную жевательную резинку и приливают 5 мл 96 % этилового спирта. Пробирку закрывают пробкой и интенсивно встряхивают в течение 1 мин. Затем смесь фильтруют и в фильтрате определяют присутствие подсластителей (сахарозы, сорбита, ксилита, маннита), являющихся многоатомными спиртами. Для этого к раствору приливают 1 мл 5-10 % раствора NaOH и 1–2 капли 10 % раствора CuSO4. Смесь взбалтывают. Появляется характерное ярко-синее окрашивание (качественная реакция на многоатомные спирты).
Раньше в качестве жвачки люди использовали смолу и высушенный сок деревьев, парафин, пчелиный воск и каучук, извлеченный из млечного сока гевеи. Традиция жевать каучук, осталась до сих пор, т.к. основой современных жевательных резинок являются каучуки. Однако сейчас их в основном получают химическим синтезом.
Следите за обновлениями!!!